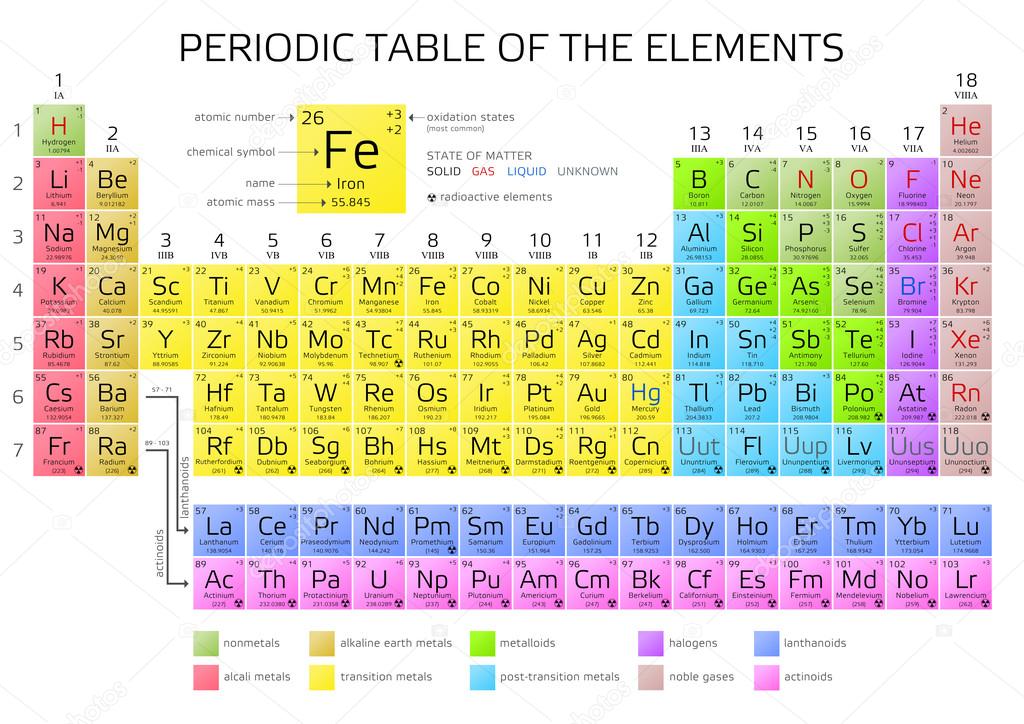
Quella Degli Elementi La Inventò Mendeleev

L'organizzazione degli elementi chimici è una pietra miliare della chimica moderna, un sistema che permette di prevedere le proprietà degli elementi e comprendere le loro relazioni. Sebbene molti scienziati abbiano contribuito allo sviluppo di questo sistema, è ampiamente riconosciuto che la Tabella Periodica, come la conosciamo oggi, sia stata significativamente influenzata dal lavoro di Dmitrij Ivanovič Mendeleev. Questo articolo esplorerà il suo contributo, i punti chiave del suo approccio e come la sua invenzione abbia rivoluzionato la chimica.
Il Contesto Storico e Scientifico
Prima di Mendeleev, diversi chimici avevano tentato di organizzare gli elementi. Le triadi di Döbereiner, ad esempio, raggruppavano elementi con proprietà simili in gruppi di tre. Altri avevano notato regolarità tra il peso atomico e le proprietà chimiche, ma nessuno era riuscito a creare un sistema comprensivo e predittivo.
Mendeleev lavorò in un'epoca in cui il numero di elementi conosciuti era in rapida crescita, e mancava una chiara comprensione delle loro relazioni. La necessità di un sistema organizzato per studiare, insegnare e prevedere le proprietà degli elementi era diventata impellente.
L'Intuizione di Mendeleev
La vera genialità di Mendeleev risiedette nella sua intuizione di ordinare gli elementi in base al loro peso atomico e di raggrupparli in base alle loro proprietà chimiche. Questo può sembrare semplice oggi, ma all'epoca era un'idea rivoluzionaria. La chiave del suo successo fu la sua volontà di lasciare degli spazi vuoti nella sua tavola, prevedendo l'esistenza di elementi ancora sconosciuti.
Mendeleev non si limitò a classificare gli elementi conosciuti; previde con accuratezza le proprietà di elementi che sarebbero stati scoperti in futuro, come il gallio (da lui chiamato eka-alluminio), il germanio (eka-silicio) e lo scandio (eka-boro). Queste previsioni audaci, che si rivelarono corrette, conferirono alla sua tavola periodica un enorme credibilità scientifica.
I Principi Fondamentali della Tavola Periodica di Mendeleev
L'organizzazione della tavola periodica di Mendeleev si basa su alcuni principi fondamentali:
- Ordinamento per Peso Atomico: Gli elementi sono disposti in ordine crescente di peso atomico.
- Raggruppamento per Proprietà Chimiche: Elementi con proprietà chimiche simili sono raggruppati verticalmente in colonne (gruppi).
- Previsione di Elementi Sconosciuti: Spazi vuoti sono lasciati per elementi non ancora scoperti, con previsioni sulle loro proprietà.
Questi principi permisero a Mendeleev di creare un sistema che non solo organizzava le conoscenze esistenti, ma che prevedeva anche nuove scoperte. La sua tavola periodica non era semplicemente una classificazione, ma uno strumento predittivo potente.
Le Correzioni e le Anomalie
È importante notare che la tavola periodica di Mendeleev non era perfetta. In alcuni casi, l'ordinamento per peso atomico portava a delle anomalie, dove elementi con proprietà simili non cadevano nello stesso gruppo. Mendeleev, in alcuni casi, invertì l'ordine di alcuni elementi per farli corrispondere alle loro proprietà chimiche, dimostrando che la somiglianza chimica era più importante del mero peso atomico.
Un esempio classico è la posizione dello iodio e del tellurio. Il tellurio ha un peso atomico maggiore dello iodio, ma le proprietà chimiche dello iodio lo collocano naturalmente nel gruppo degli alogeni, mentre il tellurio appartiene ai calcogeni. La tavola periodica moderna, basata sul numero atomico (il numero di protoni nel nucleo), risolve queste anomalie.
Dalla Massa Atomica al Numero Atomico
La comprensione moderna della tavola periodica si basa sul numero atomico, non sul peso atomico. La scoperta dei protoni e degli elettroni ha permesso di comprendere che il numero atomico determina l'identità di un elemento e le sue proprietà chimiche. Henry Moseley, tramite i suoi esperimenti con i raggi X, dimostrò che le proprietà degli elementi variavano periodicamente con il numero atomico, non con la massa atomica.
La tavola periodica moderna, quindi, è un affinamento del lavoro di Mendeleev, basato su una comprensione più profonda della struttura atomica. Anche se Mendeleev non conosceva i protoni o gli elettroni, la sua intuizione fondamentale di organizzare gli elementi in base alle loro proprietà chimiche si è rivelata corretta.
Impatto sulla Chimica e Oltre
La tavola periodica ha avuto un impatto profondo sulla chimica e su altri campi scientifici. Ha fornito un quadro concettuale per comprendere le relazioni tra gli elementi, prevedere le proprietà di nuovi materiali e progettare nuove reazioni chimiche. La sua influenza si estende dalla ricerca di base alla tecnologia avanzata.
Ad esempio, la comprensione delle proprietà degli elementi del gruppo dei metalli di transizione ha permesso lo sviluppo di catalizzatori efficienti per l'industria chimica. La conoscenza delle proprietà dei gas nobili ha portato all'utilizzo di questi elementi in illuminazione e in altre applicazioni tecnologiche. Lo sviluppo di semiconduttori si basa sulla comprensione delle proprietà degli elementi del gruppo del silicio e del germanio.
Esempi Concreti e Applicazioni Pratiche
Consideriamo alcuni esempi concreti dell'importanza della tavola periodica:
- Sintesi di nuovi elementi: La tavola periodica guida la ricerca e la sintesi di nuovi elementi superpesanti. Gli scienziati utilizzano la tavola periodica per prevedere le proprietà di questi elementi e per progettare esperimenti per la loro sintesi.
- Sviluppo di nuovi materiali: La tavola periodica è uno strumento essenziale per la progettazione di nuovi materiali con proprietà specifiche. Ad esempio, la comprensione delle proprietà degli elementi delle terre rare ha portato allo sviluppo di magneti potenti utilizzati in motori elettrici e generatori eolici.
- Medicina: Molti elementi sono essenziali per la vita e vengono utilizzati in medicina. Il ferro è un componente essenziale dell'emoglobina, il calcio è importante per la salute delle ossa, e lo iodio è necessario per il funzionamento della tiroide. La tavola periodica aiuta a comprendere il ruolo di questi elementi nel corpo umano e a sviluppare nuovi farmaci.
Questi sono solo alcuni esempi di come la tavola periodica, basata sull'intuizione di Mendeleev, continui a essere uno strumento essenziale per la scienza e la tecnologia.
Un Esempio Dettagliato: Il Gallio
Il gallio è un esempio perfetto della capacità predittiva della tavola periodica di Mendeleev. Mendeleev predisse l'esistenza di un elemento che chiamò "eka-alluminio", situato sotto l'alluminio nella sua tavola. Previde accuratamente che questo elemento avrebbe una densità relativamente bassa, un punto di fusione basso e che formerebbe un ossido con la formula X₂O₃. Quando il gallio fu scoperto nel 1875, le sue proprietà corrisposero quasi perfettamente alle previsioni di Mendeleev. Il punto di fusione basso del gallio (circa 30°C) è particolarmente notevole: può fondere nel palmo della mano. Questa proprietà, insieme alla sua buona conducibilità elettrica, lo rende utile in alcune applicazioni elettroniche.
Conclusione
Dmitrij Ivanovič Mendeleev non inventò gli elementi, ma inventò un sistema per organizzarli e comprenderli. La sua tavola periodica, pur con le sue imperfezioni iniziali, ha rivoluzionato la chimica e ha fornito un quadro concettuale essenziale per la scienza moderna. La sua intuizione di ordinare gli elementi in base al peso atomico e alle proprietà chimiche, e la sua audace previsione di elementi sconosciuti, lo consacrano come uno dei più grandi scienziati della storia.
La tavola periodica continua ad evolversi con la scoperta di nuovi elementi e con una comprensione sempre più profonda delle proprietà degli elementi esistenti. Tuttavia, i principi fondamentali stabiliti da Mendeleev rimangono validi. La prossima volta che vedete una tavola periodica, ricordatevi del genio di Dmitrij Ivanovič Mendeleev e del suo contributo inestimabile alla scienza.
Invitiamo tutti, studenti, insegnanti e appassionati di scienza, ad approfondire la conoscenza della tavola periodica. Esplorate le proprietà dei diversi elementi, scoprite le loro applicazioni e lasciatevi ispirare dalla bellezza e dalla complessità del mondo chimico. La comprensione della tavola periodica è fondamentale per comprendere il mondo che ci circonda.