Da Cosa è Formato Un Atomo
Il concetto di atomo, l'unità fondamentale della materia, ha subito un'evoluzione notevole nel corso dei secoli. Da semplici speculazioni filosofiche nell'antica Grecia, siamo arrivati a una comprensione dettagliata della sua struttura interna, grazie a progressi significativi nella fisica e nella chimica. Comprendere da cosa è formato un atomo è cruciale per comprendere il mondo che ci circonda, dalle reazioni chimiche che sostengono la vita alla tecnologia che alimenta la nostra società.
I Componenti Fondamentali dell'Atomo
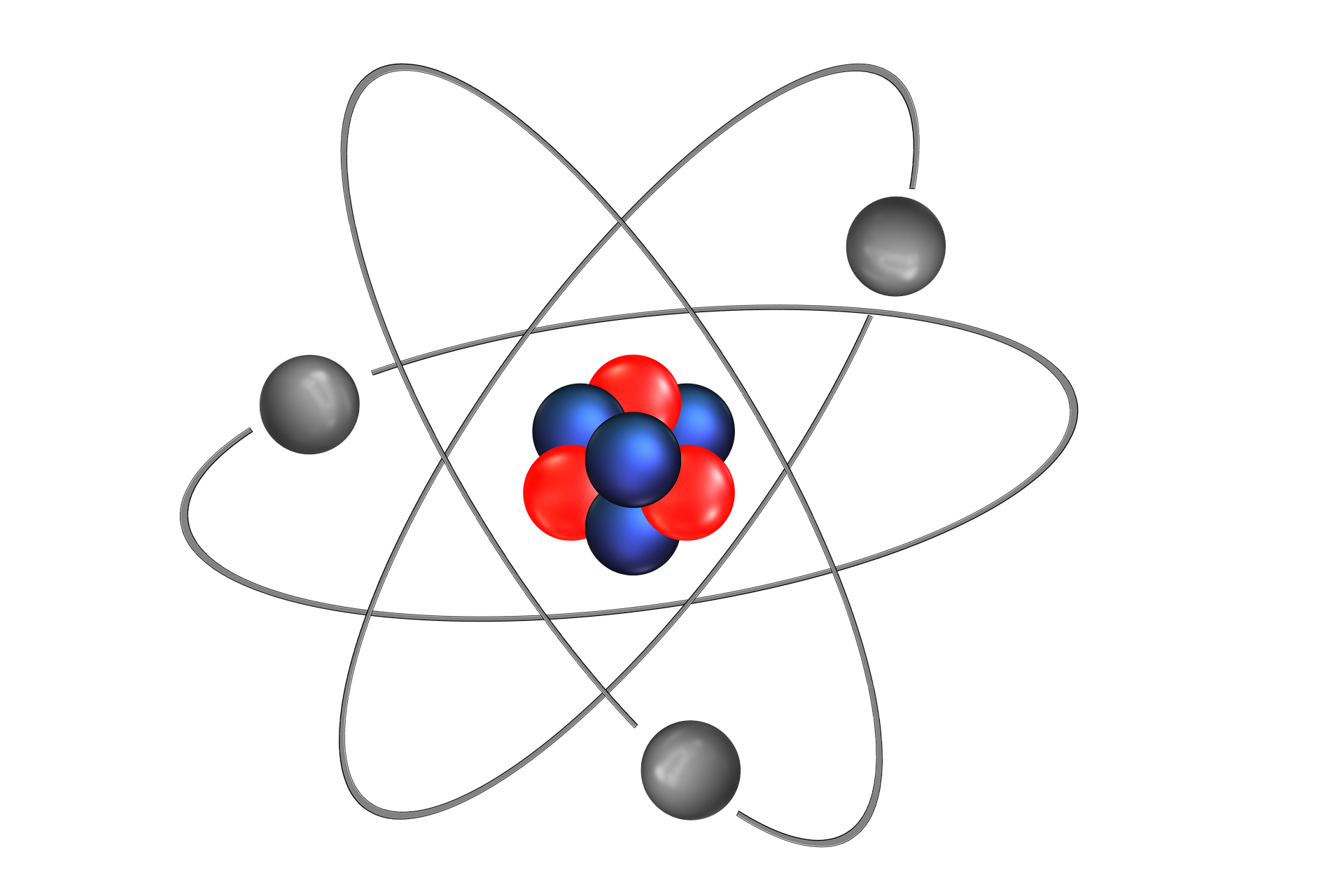
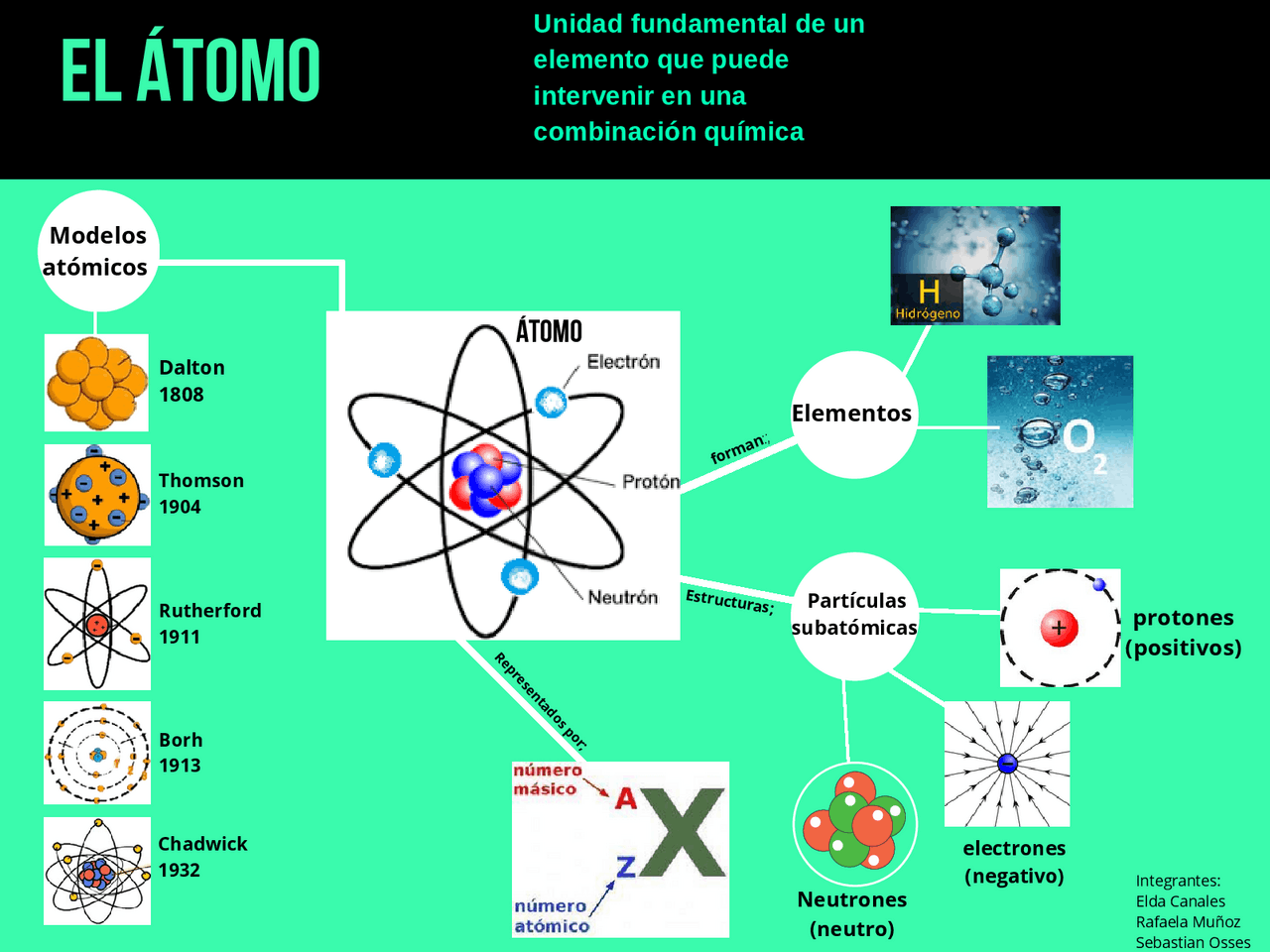
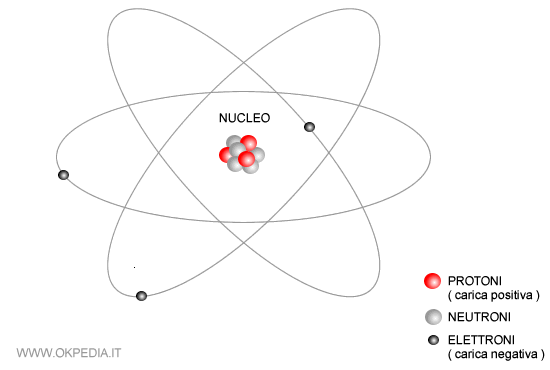
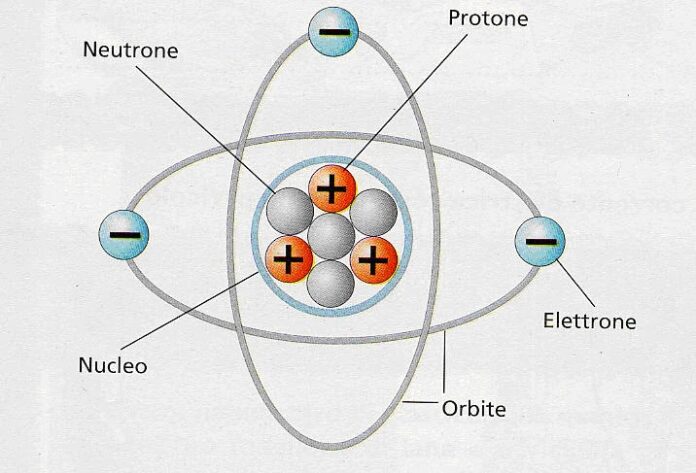
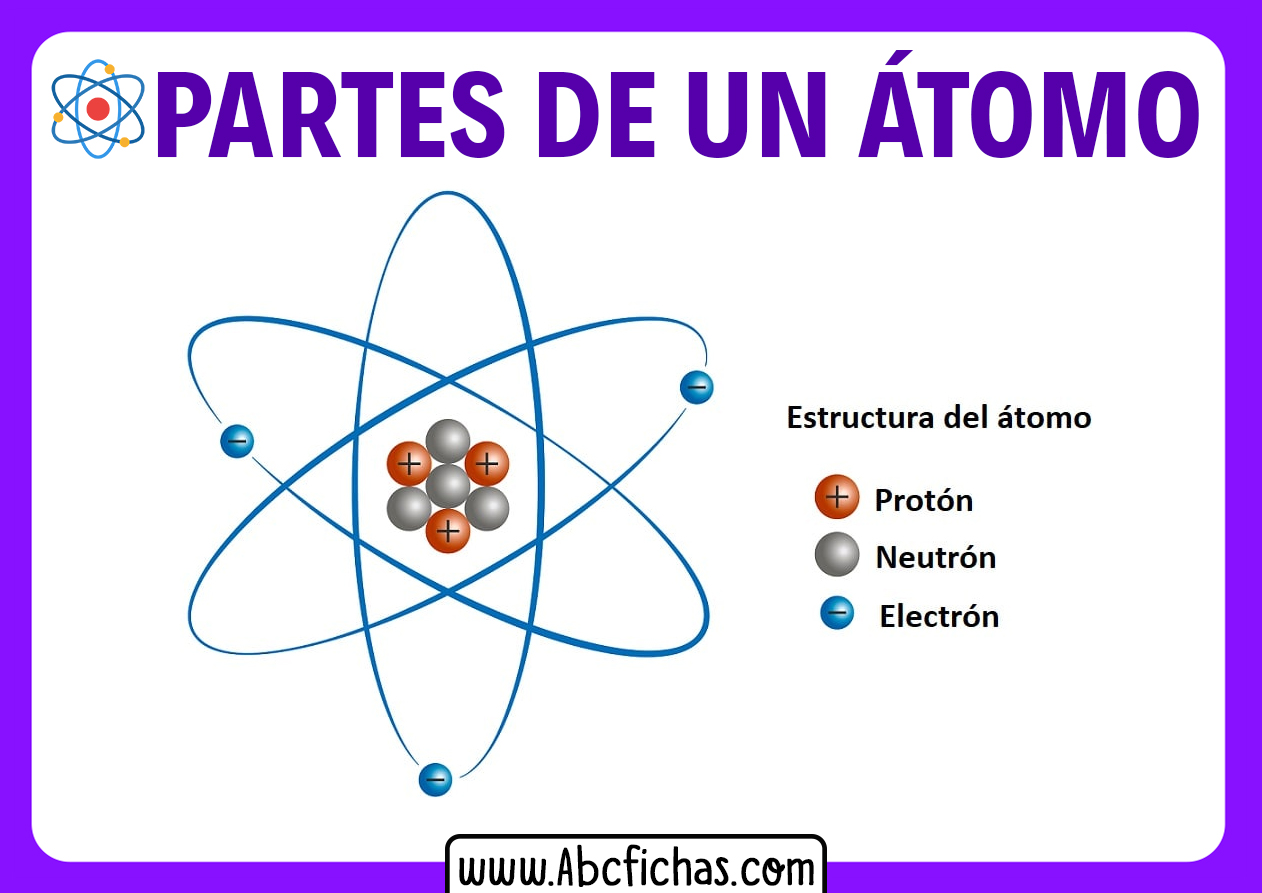
Un atomo, nella sua forma più semplice, è composto da tre tipi principali di particelle subatomiche: i protoni, i neutroni e gli elettroni. La disposizione e le proprietà di queste particelle determinano il comportamento chimico e fisico di un elemento.
Il Nucleo Atomico: Protoni e Neutroni
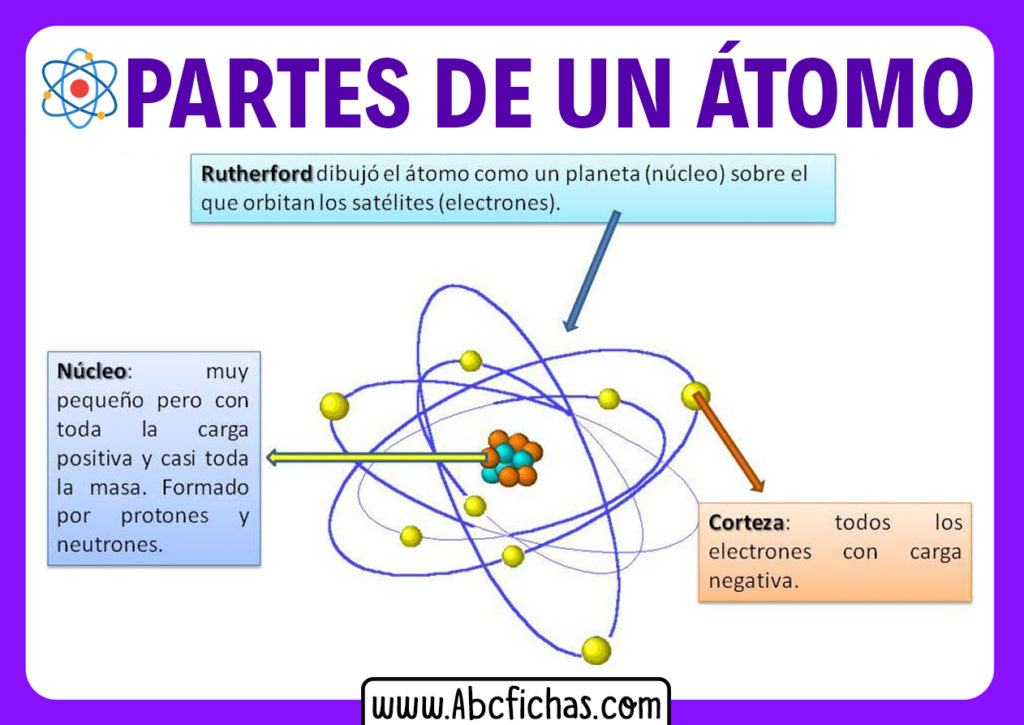
Il cuore dell'atomo è il nucleo, una regione estremamente densa che contiene i protoni e i neutroni. Queste particelle sono molto più pesanti degli elettroni. La maggior parte della massa di un atomo risiede proprio nel suo nucleo.
I protoni sono particelle con carica elettrica positiva. Il numero di protoni nel nucleo determina l'elemento chimico a cui l'atomo appartiene. Ad esempio, un atomo con un protone è idrogeno, un atomo con sei protoni è carbonio, e così via. Questo numero, chiamato numero atomico (simbolo Z), è l'identificatore univoco di ogni elemento nella tavola periodica.
I neutroni, come suggerisce il nome, sono particelle neutre, cioè prive di carica elettrica. La loro funzione principale è quella di contribuire alla stabilità del nucleo. I neutroni esercitano una forza nucleare forte che contrasta la repulsione elettromagnetica tra i protoni, impedendo al nucleo di disintegrarsi. Atomi dello stesso elemento con un numero diverso di neutroni sono chiamati isotopi. Ad esempio, il carbonio-12 (12C) ha 6 protoni e 6 neutroni, mentre il carbonio-14 (14C) ha 6 protoni e 8 neutroni. Entrambi sono carbonio, ma con masse diverse.
Gli Elettroni: Il Guscio Elettronico
Gli elettroni sono particelle con carica elettrica negativa che orbitano attorno al nucleo. A differenza dei protoni e dei neutroni, gli elettroni sono estremamente leggeri. La massa di un elettrone è circa 1/1836 della massa di un protone.
Gli elettroni non orbitano il nucleo in traiettorie fisse e definite, come i pianeti attorno al sole. Invece, occupano orbitali atomici, regioni di spazio attorno al nucleo dove è più probabile trovare un elettrone. Questi orbitali sono organizzati in gusci elettronici o livelli di energia. Il guscio più vicino al nucleo (il primo guscio) può contenere al massimo due elettroni, mentre i gusci successivi possono contenere un numero maggiore di elettroni.
La disposizione degli elettroni nei gusci elettronici determina le proprietà chimiche di un atomo. Gli atomi con un guscio esterno incompleto tendono a reagire con altri atomi per raggiungere una configurazione stabile, con un guscio esterno completo. Questo è il principio alla base del legame chimico.
Forze Fondamentali all'Opera
La stabilità di un atomo è il risultato dell'interazione di diverse forze fondamentali:
* Forza elettromagnetica: Questa forza attrae gli elettroni (carica negativa) al nucleo (carica positiva) e respinge i protoni tra loro. * Forza nucleare forte: Questa forza è molto più potente della forza elettromagnetica a brevi distanze ed è responsabile di tenere insieme i protoni e i neutroni nel nucleo. * Forza nucleare debole: Questa forza è responsabile di alcuni tipi di decadimento radioattivo, in cui un neutrone può trasformarsi in un protone e un elettrone (e un antineutrino).Esempi Reali e Applicazioni
La conoscenza della struttura atomica è fondamentale per una vasta gamma di applicazioni in diversi campi:
* Medicina: La radioterapia utilizza radiazioni ionizzanti per distruggere le cellule tumorali, sfruttando la capacità delle radiazioni di danneggiare il DNA. La risonanza magnetica (RM) si basa sulle proprietà magnetiche dei nuclei atomici per creare immagini dettagliate degli organi interni. * Energia: L'energia nucleare viene prodotta attraverso la fissione nucleare, in cui nuclei di atomi pesanti (come l'uranio) vengono scissi per liberare energia. La fusione nucleare, che unisce nuclei di atomi leggeri per formare nuclei più pesanti, è la fonte di energia del sole e delle stelle e rappresenta una potenziale fonte di energia pulita per il futuro. * Scienza dei materiali: La comprensione della struttura atomica dei materiali permette di progettare nuovi materiali con proprietà specifiche, come alta resistenza, leggerezza, o conducibilità elettrica. Ad esempio, i semiconduttori utilizzati nei computer e nei telefoni cellulari sono realizzati manipolando la struttura atomica di elementi come il silicio. * Datazione al radiocarbonio: Misurando la quantità di carbonio-14 (un isotopo radioattivo del carbonio) in un campione organico, è possibile determinare la sua età. Questa tecnica è utilizzata in archeologia e geologia per datare reperti storici e campioni geologici. L'emivita del Carbonio-14 è di circa 5730 anni. Ciò significa che dopo 5730 anni, la metà degli atomi di Carbonio-14 in un campione si sarà trasformata in azoto.Oltre l'Atomo: Le Particelle Elementari
La nostra comprensione della materia non si ferma all'atomo. I protoni e i neutroni, una volta considerati particelle fondamentali, sono in realtà composti da particelle ancora più piccole chiamate quark. Gli elettroni, invece, sono considerati particelle elementari, cioè non composte da particelle più piccole. La fisica delle particelle studia queste particelle elementari e le forze che le governano, cercando di svelare i misteri più profondi dell'universo.
Conclusione
L'atomo, con la sua complessa struttura e le sue proprietà uniche, è la pietra angolare della materia. Comprendere da cosa è formato un atomo è essenziale per sbloccare nuove tecnologie e risolvere i problemi più pressanti del nostro tempo, dalla produzione di energia pulita allo sviluppo di nuovi farmaci. La ricerca sulla struttura atomica continua ad evolversi, offrendo nuove prospettive sulla natura fondamentale della realtà. Invitiamo tutti a esplorare ulteriormente questo affascinante campo della scienza e a contribuire alla nostra continua comprensione dell'universo.