Cosa Dice Il Secondo Principio Della Termodinamica

Avete mai provato a riordinare la vostra stanza, solo per ritrovarla di nuovo in disordine qualche giorno dopo? Oppure vi siete chiesti perché un cubetto di ghiaccio si scioglie in un bicchiere d'acqua calda, ma l'acqua calda non si congela spontaneamente in un cubetto di ghiaccio? La risposta a queste domande si trova in un principio fondamentale della fisica: il secondo principio della termodinamica.
Questo articolo, rivolto a chiunque sia curioso di capire meglio come funziona il mondo che ci circonda, esplorerà in dettaglio questo principio. Cercheremo di renderlo accessibile e comprensibile, anche per chi non ha una formazione scientifica approfondita.
Cos'è la Termodinamica?
Prima di addentrarci nel secondo principio, è utile definire cos'è la termodinamica. In parole semplici, la termodinamica è lo studio dell'energia e delle sue trasformazioni. Si occupa di come il calore, il lavoro e l'energia interna sono interconnessi e di come questi influenzano lo stato della materia.
Immaginate un motore a combustione interna. La termodinamica studia come l'energia chimica del carburante viene convertita in calore, e come questo calore viene poi trasformato in lavoro meccanico per far muovere l'auto. Oppure, pensate al vostro frigorifero: la termodinamica spiega come esso utilizza l'energia per rimuovere il calore dall'interno, mantenendo il cibo fresco.
Il Primo Principio: Conservazione dell'Energia
Per comprendere appieno il secondo principio, è importante conoscere anche il primo principio della termodinamica, che afferma che l'energia si conserva. Questo significa che l'energia non può essere creata né distrutta, ma solo trasformata da una forma all'altra.
Ad esempio, quando accendete una lampadina, l'energia elettrica viene trasformata in energia luminosa e calore. La quantità totale di energia rimane costante: l'energia elettrica in ingresso è uguale alla somma dell'energia luminosa e del calore in uscita.
Tuttavia, il primo principio non ci dice nulla sulla *direzione* di queste trasformazioni. Potrebbe sembrare che qualsiasi trasformazione che conservi l'energia sia possibile, ma l'esperienza quotidiana ci dimostra che non è così. Ed è qui che entra in gioco il secondo principio.
Il Secondo Principio: Entropia e Irreversibilità
Il secondo principio della termodinamica introduce il concetto di entropia. L'entropia è una misura del *disordine* o della *casualità* di un sistema. In termini più tecnici, è una misura del numero di microstati possibili che corrispondono a un dato macrostato. Maggiore è il numero di microstati possibili, maggiore è l'entropia.
Il secondo principio afferma che l'entropia di un sistema isolato tende ad aumentare nel tempo, o al massimo a rimanere costante. In altre parole, i sistemi isolati tendono spontaneamente verso uno stato di maggiore disordine. Questo è il motivo per cui la vostra stanza si disordina da sola, e perché un cubetto di ghiaccio si scioglie in acqua calda.
Proviamo a visualizzare questo concetto. Immaginate un mazzo di carte perfettamente ordinato per seme e valore. Se lo lanciate in aria, è estremamente improbabile che le carte ricadano esattamente nello stesso ordine. Piuttosto, è molto più probabile che si disperdano casualmente sul pavimento. Questo perché ci sono molti più modi possibili per disporre le carte in modo disordinato che in modo ordinato.
Un'altra conseguenza del secondo principio è l'irreversibilità dei processi. Molti processi fisici avvengono spontaneamente in una direzione, ma non nell'altra. Ad esempio:
- Il calore fluisce spontaneamente da un corpo caldo a un corpo freddo, ma non viceversa.
- Un gas si espande spontaneamente per riempire un volume disponibile, ma non si comprime spontaneamente in un volume più piccolo.
- Un pendolo oscilla, ma a causa dell'attrito, la sua oscillazione diminuisce gradualmente fino a fermarsi. L'energia cinetica del pendolo si trasforma in calore, che si disperde nell'ambiente.
Questi processi sono irreversibili perché richiederebbero una diminuzione dell'entropia per avvenire nella direzione opposta, il che violerebbe il secondo principio.
Esempi Pratici del Secondo Principio
Il secondo principio della termodinamica ha implicazioni innumerevoli nella nostra vita quotidiana e in diversi campi scientifici. Ecco alcuni esempi:
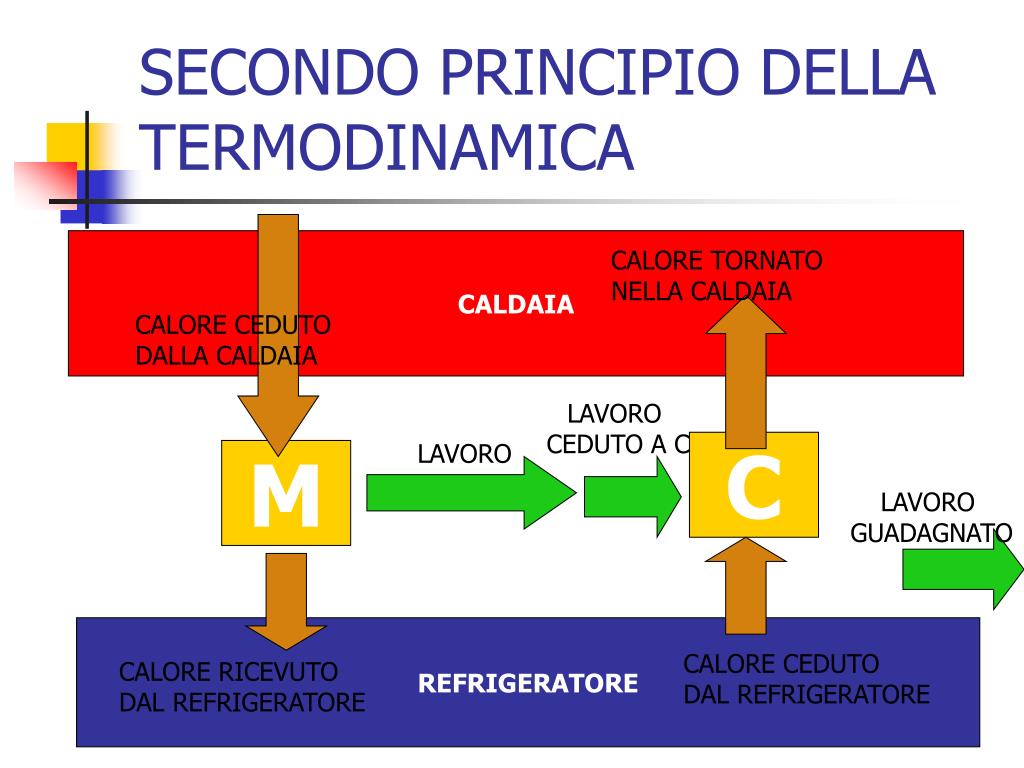
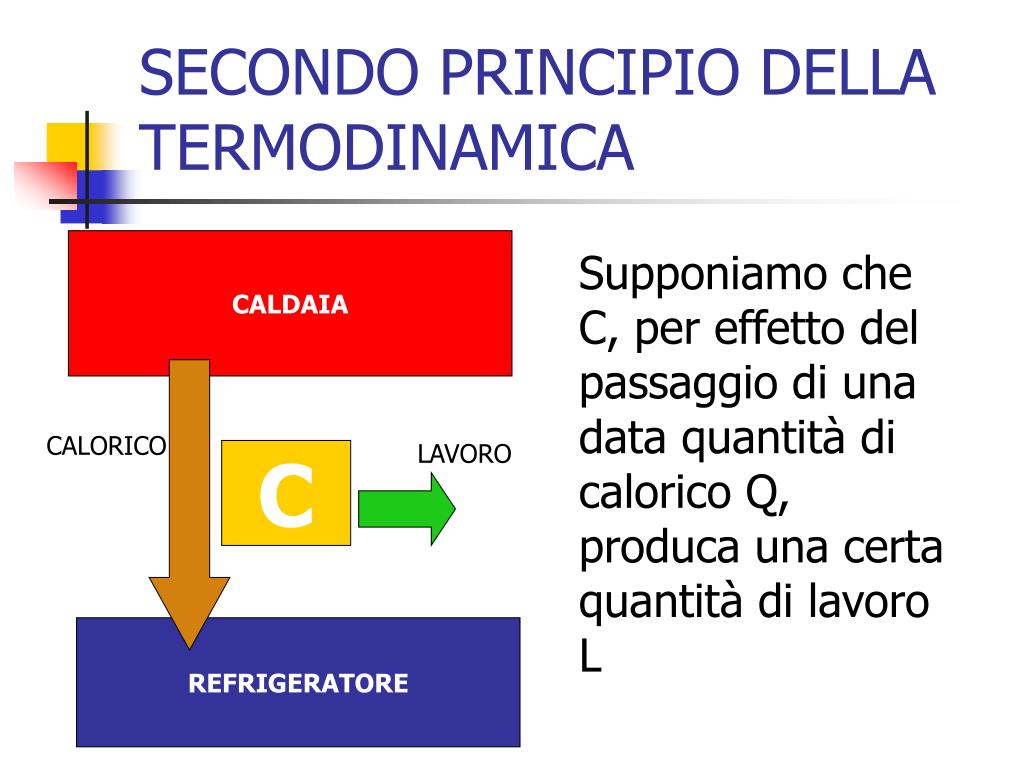
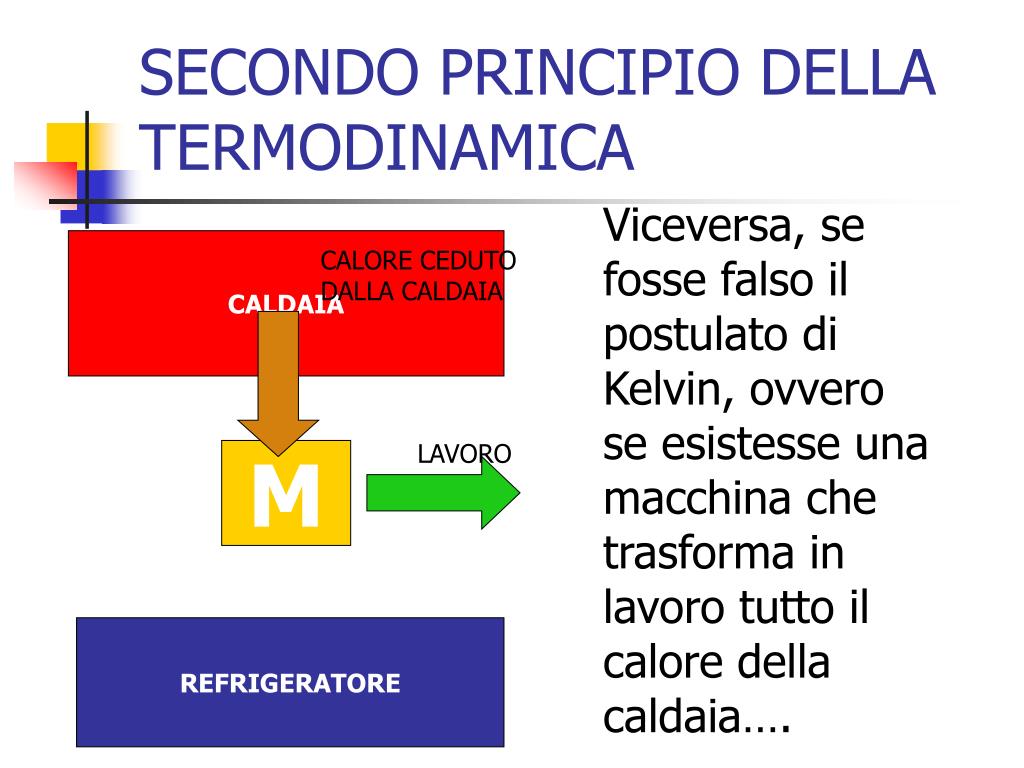
- Motori termici: I motori termici, come quelli delle automobili o delle centrali elettriche, convertono il calore in lavoro. Il secondo principio impone un limite all'efficienza di questi motori. Non è possibile convertire tutto il calore in lavoro; una parte di esso deve essere scaricata come calore di scarto, aumentando l'entropia dell'ambiente.
- Refrigerazione: I frigoriferi e i condizionatori d'aria trasferiscono il calore da un ambiente freddo a uno caldo, il che sembra violare il secondo principio. Tuttavia, questi dispositivi richiedono un apporto di energia esterna per funzionare, e questo processo aumenta l'entropia complessiva del sistema (frigorifero + ambiente).
- Chimica: Il secondo principio aiuta a prevedere la spontaneità delle reazioni chimiche. Le reazioni che aumentano l'entropia del sistema tendono ad avvenire spontaneamente.
- Cosmologia: Il secondo principio gioca un ruolo importante nella nostra comprensione dell'evoluzione dell'universo. L'universo tende verso uno stato di massima entropia, noto come "morte termica", in cui tutta l'energia sarà uniformemente distribuita e non sarà più possibile eseguire alcun lavoro.
La Relazione tra Entropia e Probabilità
Un modo più intuitivo per capire l'entropia è considerarla come una misura della probabilità. Gli stati con alta entropia sono più probabili degli stati con bassa entropia. Questo perché ci sono molti più modi per ottenere uno stato disordinato che uno stato ordinato.
Immaginate di lanciare una moneta 10 volte. È possibile ottenere una sequenza di "testa" o "croce" perfettamente alternata (ad esempio, TCTCTCTCTC). Tuttavia, questa è solo una delle 1024 (2^10) sequenze possibili. La stragrande maggioranza delle sequenze sarà una miscela casuale di "testa" e "croce". Quindi, una sequenza casuale è molto più probabile di una sequenza ordinata.
Entropia e Vita
La vita sembra essere una violazione del secondo principio, perché gli organismi viventi sono altamente ordinati e complessi. Tuttavia, la vita non viola il secondo principio perché gli organismi viventi non sono sistemi isolati. Essi scambiano energia e materia con l'ambiente circostante.
Gli organismi viventi mantengono il loro ordine interno aumentando l'entropia dell'ambiente. Ad esempio, le piante assorbono l'energia solare e la usano per sintetizzare molecole complesse come il glucosio. Questo processo riduce l'entropia all'interno della pianta, ma aumenta l'entropia dell'ambiente circostante rilasciando calore e ossigeno (che è più disordinato dell'anidride carbonica). In sostanza, la vita crea ordine al suo interno "scaricando" disordine nell'ambiente circostante.
Il Secondo Principio e Noi
Capire il secondo principio della termodinamica non è solo interessante dal punto di vista scientifico, ma può anche influenzare il nostro modo di pensare al mondo. Ci ricorda che l'ordine richiede sforzo e che il disordine è la condizione naturale a cui tendono i sistemi isolati. Ci insegna a valorizzare l'energia e a utilizzarla in modo efficiente, perché ogni trasformazione energetica comporta una perdita di energia utile a causa dell'aumento dell'entropia.
Forse, la prossima volta che vi lamenterete del disordine nella vostra stanza, vi ricorderete del secondo principio e lo accetterete come una legge fondamentale dell'universo. Oppure, forse, vi sentirete motivati a contrastare temporaneamente questa legge, impiegando un po' di energia per riportare l'ordine! Ogni piccolo gesto conta per ridurre l'aumento dell'entropia!
In definitiva, il secondo principio della termodinamica ci offre una prospettiva umile e affascinante sul nostro posto nell'universo. Ci ricorda che siamo parte di un sistema più grande, in continua evoluzione verso uno stato di maggiore disordine. Comprendere questo principio ci aiuta a navigare meglio nel mondo che ci circonda e a prendere decisioni più consapevoli riguardo all'uso delle risorse e alla conservazione dell'energia. E questo è un valore inestimabile.