Chimica Concetti E Modelli Dalla Materia All'atomo

Capita a tutti, prima o poi, di trovarsi di fronte alla chimica e sentirsi sopraffatti. Forse è un ricordo delle lezioni a scuola, piene di formule incomprensibili e termini astrusi. Forse è la complessità del mondo che ci circonda, fatto di molecole che interagiscono in modi che ci sfuggono. Qualunque sia la ragione, la chimica può sembrare una barriera insormontabile. Ma non deve essere così.
L'obiettivo di questo articolo è quello di demistificare la chimica, partendo dai suoi concetti fondamentali e costruendo gradualmente una solida comprensione della materia e degli atomi. Non si tratta di memorizzare formule, ma di capire i principi che regolano il comportamento della materia. In fin dei conti, la chimica è ovunque: nel cibo che mangiamo, nell'aria che respiriamo, nei materiali che usiamo ogni giorno. Comprendere la chimica significa comprendere il mondo che ci circonda.
La Materia: Oltre l'Apparenza
La materia è tutto ciò che ha massa e occupa spazio. Può essere solida, liquida, gassosa o plasma. Ma cosa c'è dentro? Cosa rende la materia così diversa in apparenza, eppure governata da leggi universali?
La risposta risiede nella sua composizione e nella sua struttura a livello atomico e molecolare. Immaginate di avere un cubetto di ghiaccio. A occhio nudo, sembra un solido trasparente. Ma se potessimo ingrandirlo a un livello incredibile, vedremmo che è composto da milioni di molecole d'acqua (H2O) tenute insieme da forze di attrazione. Quando il ghiaccio si scioglie, queste forze si indeboliscono e le molecole si muovono più liberamente, trasformando il solido in liquido. Se scaldiamo ulteriormente l'acqua, le molecole acquisiscono ancora più energia e si allontanano completamente le une dalle altre, trasformando il liquido in vapore.
Questo esempio illustra un concetto fondamentale: lo stato della materia dipende dall'energia cinetica delle molecole e dalle forze che le tengono unite.
Ma da cosa sono fatte le molecole?
Gli Elementi: I Mattoni Fondamentali
Le molecole sono composte da atomi, e gli atomi sono gli elementi fondamentali della materia. Un elemento è una sostanza che non può essere scomposta in sostanze più semplici con mezzi chimici. Esistono 118 elementi conosciuti, ognuno con le sue proprietà uniche. Questi elementi sono organizzati nella tavola periodica, uno strumento cruciale per comprendere le relazioni tra gli elementi e le loro proprietà.
La tavola periodica non è solo un elenco di elementi; è una mappa che rivela i modelli nel comportamento chimico. Gli elementi nello stesso gruppo (colonna verticale) hanno proprietà simili perché hanno lo stesso numero di elettroni nel loro guscio esterno, che è il guscio che determina come un atomo reagirà con altri atomi.
Ad esempio, il sodio (Na) e il potassio (K) sono entrambi metalli alcalini. Reagiscono violentemente con l'acqua per formare idrossido di sodio (NaOH) e idrossido di potassio (KOH), rispettivamente, liberando idrogeno gassoso. Questa somiglianza nel comportamento è dovuta al fatto che entrambi gli elementi hanno un solo elettrone nel loro guscio esterno.
L'Atomo: Il Nucleo della Materia
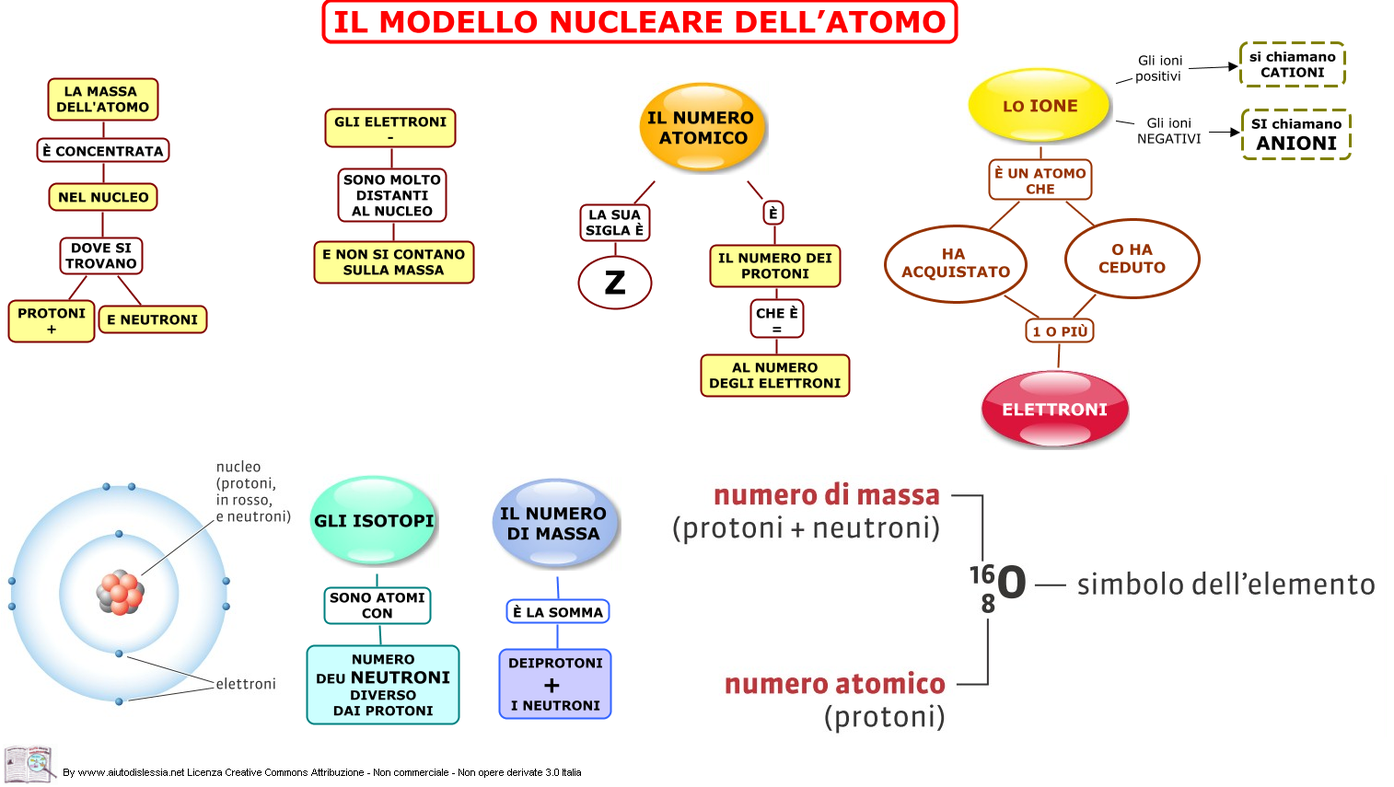
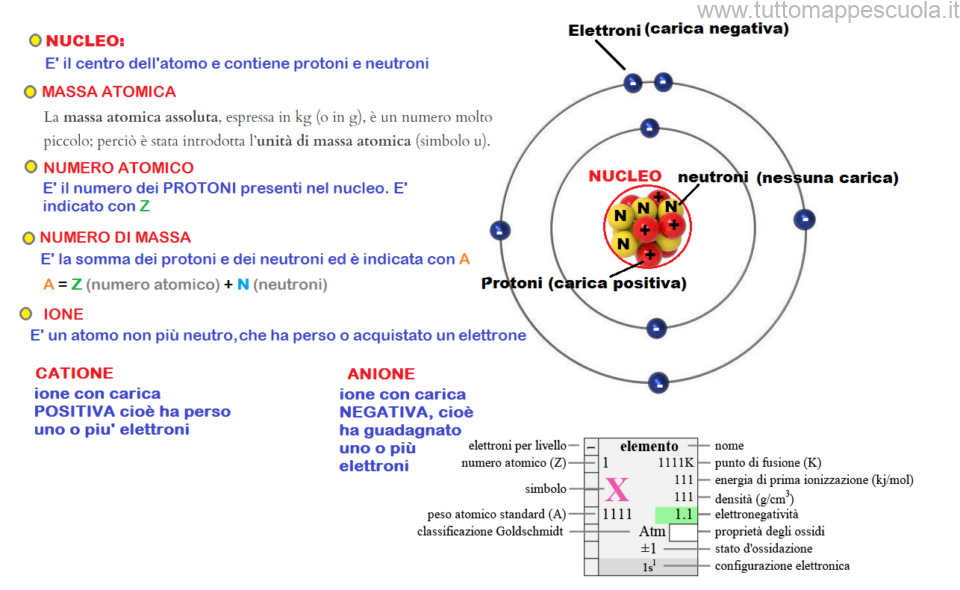
L'atomo è la più piccola unità di un elemento che conserva le proprietà chimiche di quell'elemento. È composto da tre particelle subatomiche principali: protoni, neutroni ed elettroni.
- I protoni hanno carica positiva e si trovano nel nucleo dell'atomo. Il numero di protoni determina l'elemento a cui appartiene l'atomo (il numero atomico).
- I neutroni non hanno carica e si trovano anch'essi nel nucleo. Aggiungono massa all'atomo, ma non influenzano la sua carica.
- Gli elettroni hanno carica negativa e orbitano attorno al nucleo in regioni chiamate orbitali. Il numero di elettroni determina le proprietà chimiche dell'atomo.
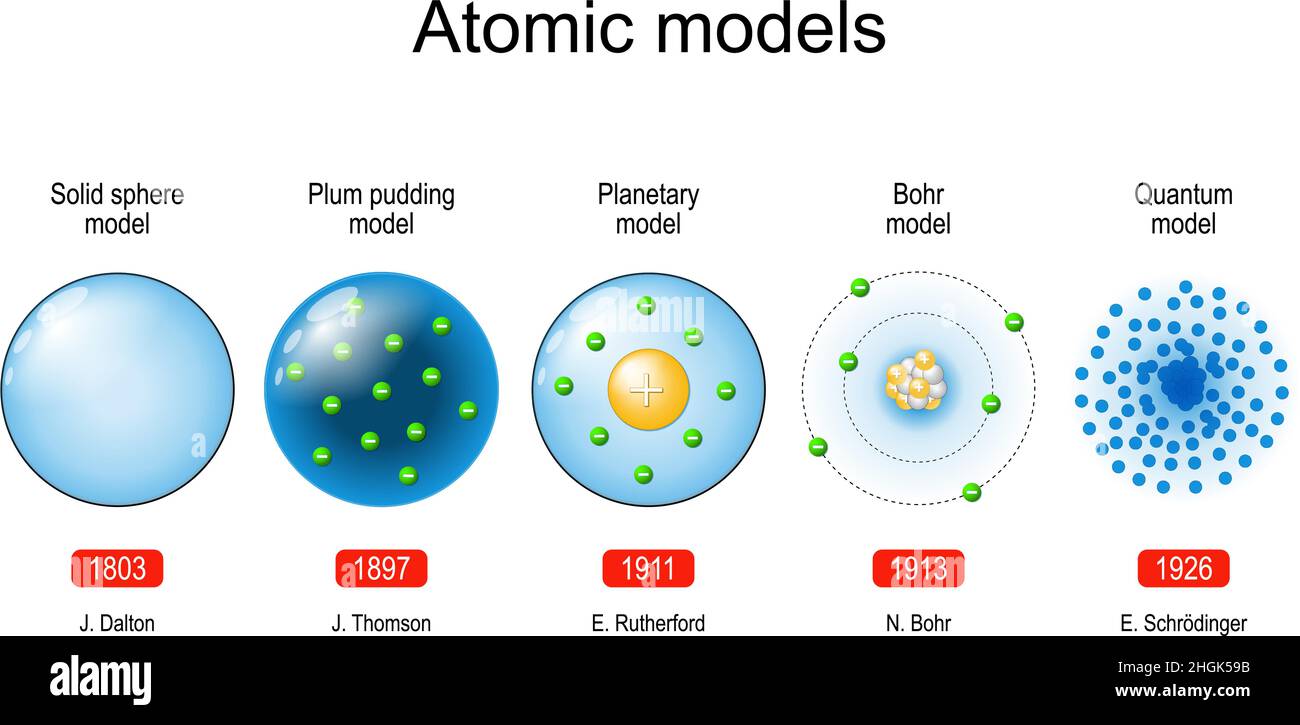
Immaginate l'atomo come un piccolo sistema solare, con il nucleo al centro (come il sole) e gli elettroni che orbitano attorno (come i pianeti). Questa è una semplificazione, ma aiuta a visualizzare la struttura dell'atomo.
Legami Chimici: Unire gli Atomi
Gli atomi non esistono solitamente da soli. Tendono a legarsi tra loro per formare molecole o composti. I legami chimici sono le forze che tengono uniti gli atomi.
Esistono diversi tipi di legami chimici, tra cui:
- Legami ionici: si formano quando un atomo cede uno o più elettroni a un altro atomo. L'atomo che cede gli elettroni diventa uno ione positivo (catione), mentre l'atomo che li riceve diventa uno ione negativo (anione). L'attrazione elettrostatica tra i due ioni forma il legame. Un esempio classico è il cloruro di sodio (NaCl), il sale da cucina, formato dal legame ionico tra lo ione sodio (Na+) e lo ione cloruro (Cl-).
- Legami covalenti: si formano quando due atomi condividono uno o più elettroni. Questo tipo di legame è comune tra atomi non metallici. Un esempio è la molecola d'acqua (H2O), in cui due atomi di idrogeno condividono elettroni con un atomo di ossigeno.
- Legami metallici: si formano tra atomi metallici. Gli elettroni vengono delocalizzati e possono muoversi liberamente attraverso la struttura del metallo, conferendogli la sua caratteristica conduttività elettrica e termica.
Il tipo di legame chimico che si forma tra gli atomi determina le proprietà del composto o della molecola risultante. Ad esempio, i composti ionici tendono ad avere punti di fusione e di ebollizione elevati, mentre i composti covalenti tendono ad avere punti di fusione e di ebollizione più bassi.
Reazioni Chimiche: Trasformazioni della Materia
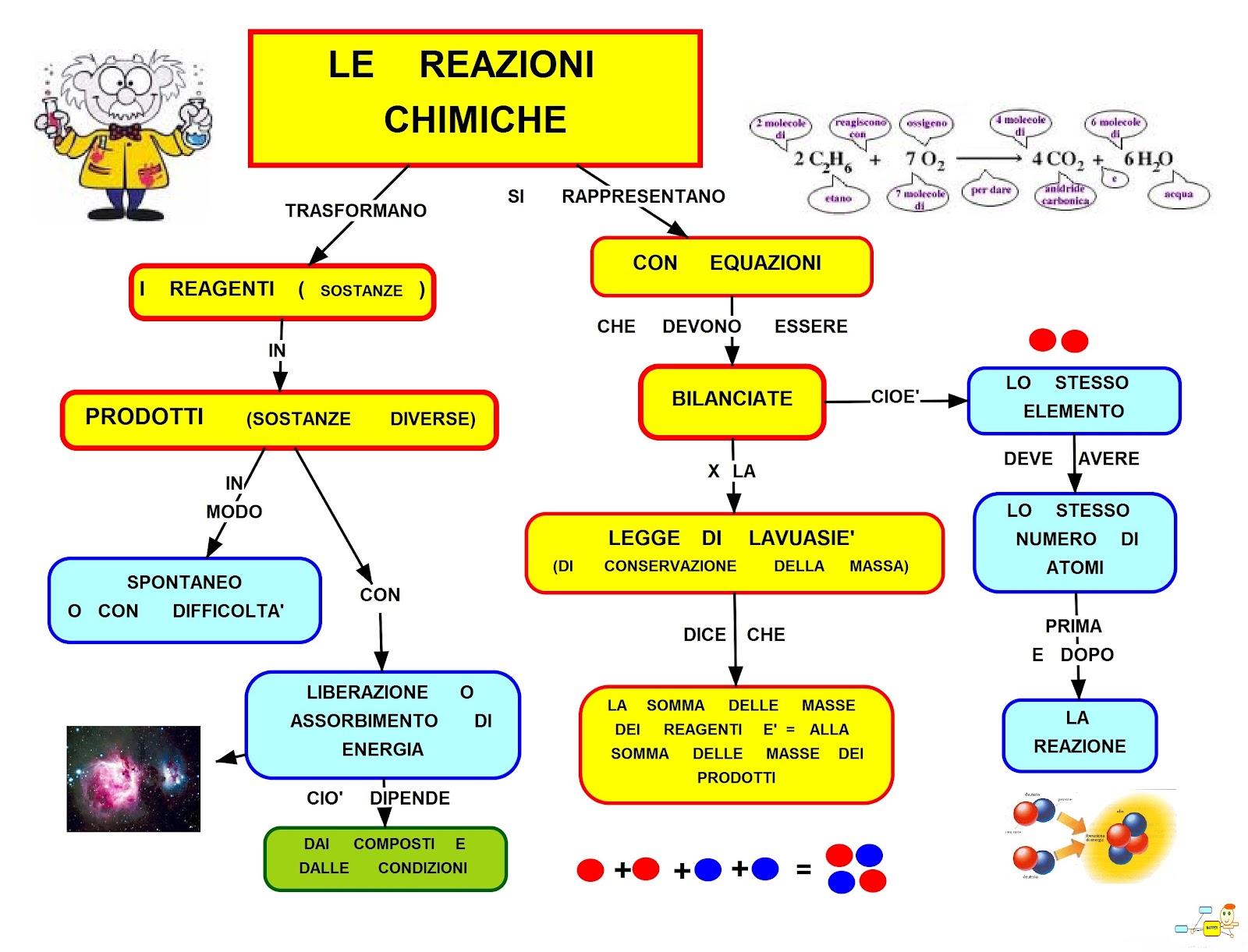
Una reazione chimica è un processo che coinvolge la rottura e la formazione di legami chimici. Durante una reazione chimica, gli atomi si riarrangiano per formare nuove sostanze.
Le reazioni chimiche sono rappresentate da equazioni chimiche, che mostrano i reagenti (le sostanze che reagiscono) e i prodotti (le sostanze che si formano). Ad esempio, la reazione tra idrogeno e ossigeno per formare acqua è rappresentata dall'equazione:
2H2 + O2 → 2H2O
Questa equazione indica che due molecole di idrogeno reagiscono con una molecola di ossigeno per formare due molecole d'acqua.
Le reazioni chimiche sono alla base di molti processi importanti, come la combustione, la respirazione, la fotosintesi e la produzione di farmaci e materiali.
Energia nelle Reazioni Chimiche
Le reazioni chimiche coinvolgono sempre variazioni di energia. Alcune reazioni rilasciano energia (reazioni esotermiche), mentre altre richiedono energia per avvenire (reazioni endotermiche). La combustione del legno è un esempio di reazione esotermica, mentre la fotosintesi è un esempio di reazione endotermica.
L'energia necessaria per avviare una reazione chimica è chiamata energia di attivazione. I catalizzatori sono sostanze che accelerano le reazioni chimiche diminuendo l'energia di attivazione.
Chimica: Più che Equazioni e Formule
La chimica non è solo un insieme di regole e definizioni astratte. È una scienza dinamica e in continua evoluzione che ci aiuta a comprendere il mondo che ci circonda e a sviluppare nuove tecnologie.
Alcuni esempi di come la chimica influisce sulla nostra vita quotidiana:
- Medicina: La chimica è fondamentale per lo sviluppo di nuovi farmaci e terapie. La comprensione della struttura e del comportamento delle molecole ci permette di progettare farmaci che interagiscono in modo specifico con le cellule del corpo, curando malattie e migliorando la qualità della vita.
- Agricoltura: La chimica è utilizzata per sviluppare fertilizzanti e pesticidi che aumentano la resa dei raccolti e proteggono le piante dalle malattie. Tuttavia, è importante utilizzare questi prodotti in modo responsabile per evitare danni all'ambiente.
- Materiali: La chimica è alla base dello sviluppo di nuovi materiali con proprietà specifiche, come plastiche resistenti, fibre leggere e superconduttori. Questi materiali sono utilizzati in una vasta gamma di applicazioni, dall'edilizia all'elettronica.
- Energia: La chimica gioca un ruolo cruciale nello sviluppo di nuove fonti di energia pulita e rinnovabile, come le celle solari e le batterie. La comprensione delle reazioni chimiche che avvengono in queste tecnologie è essenziale per migliorarne l'efficienza e la durata.
Alcuni potrebbero obiettare che la chimica è pericolosa a causa degli incidenti industriali e dell'inquinamento. Questo è un punto valido, ma è importante ricordare che la chimica è uno strumento. Come tutti gli strumenti, può essere usato per il bene o per il male. La chiave è utilizzarla in modo responsabile e sostenibile, tenendo conto dell'impatto sull'ambiente e sulla salute umana.
Comprendere i concetti fondamentali della chimica non è solo utile per gli studenti o i ricercatori. È importante per tutti i cittadini, perché ci permette di prendere decisioni informate su questioni che riguardano la nostra salute, l'ambiente e il futuro del nostro pianeta.
Speriamo che questo articolo vi abbia fornito una solida base per comprendere la chimica. Ricordate, la chimica è ovunque. Osservate il mondo che vi circonda con occhi nuovi e cercate di individuare le reazioni chimiche che avvengono continuamente. La chimica è la chiave per comprendere il mondo, e comprendere il mondo è la chiave per migliorare la nostra vita.
Ora, cosa vi incuriosisce di più della chimica? Quali domande vi siete sempre posti e a cui vorreste trovare risposta?